再鼎医药公布2023年第三季度财务业绩和公司进展
- 2023年第三季度的产品总收入为6,920万美元,同比增长22%;按固定汇率计算同比增长27%
- 卫伟迦®(艾加莫德α注射液)自9月在中国商业化上市以来,实现销售收入490万美元
- 稳健的资产负债状况,截至2023年9月30日现金储备为8.222亿美元,而截至2023年6月30日为8.764亿美元
- 公司将于美国东部时间2023年11月8日上午8:00举行电话会议和网络直播
中国上海和美国马萨诸塞州剑桥市,2023年11月7日——再鼎医药(纳斯达克股票代码:ZLAB;香港联交所股份代号:9688),今日公布了2023年第三季度的财务业绩,以及近期的产品亮点和公司进展。
再鼎医药创始人、董事长兼首席执行官杜莹博士表示:“2023年第三季度,我们实现了多个重要里程碑,包括在中国成功上市卫伟迦用于治疗全身型重症肌无力(gMG)患者,以及艾加莫德用于慢性炎性脱髓鞘性多发性神经根神经病(CIDP)的关键性临床研究取得阳性结果。这些进展突显了我们坚定不移为亟需患者提供创新药物的承诺。国家药品监督管理局(NMPA)正在审评审批我们的多个新药上市申请和正在进行的具有重大市场潜力药物的关键性临床研究,我们拥有良好优势,以加速我们的管线进展和拓展我们商业化产品组合,为全球患者带来更多福祉。”
再鼎医药总裁兼首席运营官Josh Smiley表示:“我们的商业化团队面对第三季度宏观层面的挑战,仍实现了同比27%的产品净收入增长(以固定汇率计算)。则乐仍然是中国内地卵巢癌领域院内销售领先PARP抑制剂;作为一款有望改变中国 gMG 患者治疗模式的药物,卫伟迦的商业化上市已展现出令人兴奋的趋势。预计在未来两到三年内,再鼎至少还将有额外的7款产品上市,有望贡献重要的收入增长。随着业务增长与运营效率的提高,将有助于我们在未来实现盈利。”
2023年第三季度财务业绩
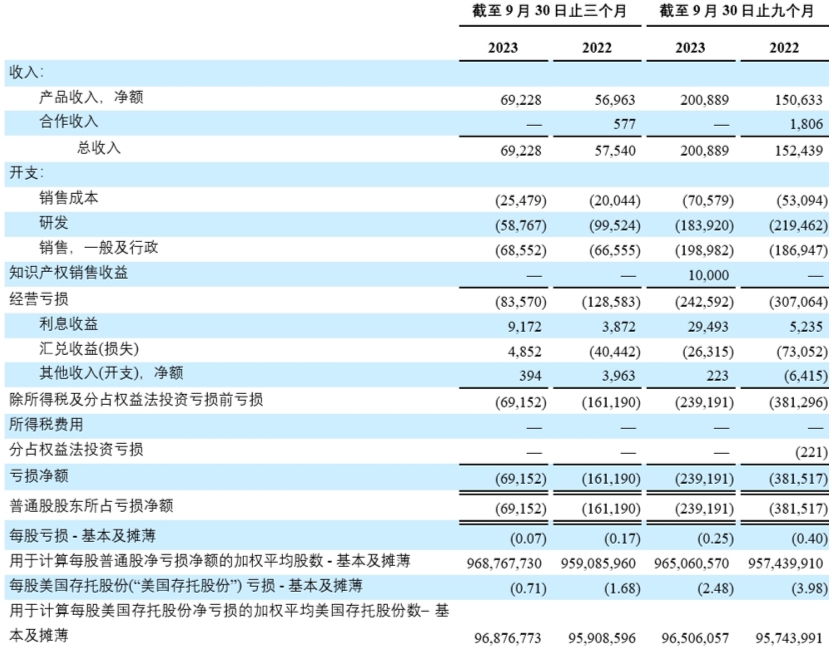
- 2023年第三季度的产品收入为6,920万美元,2022年同期为5,700万美元,同比增长22%,按固定汇率计算同比增长27%。产品收入增加主要是由于销量的增加、卫伟迦的上市以及COVID-19疫情负面影响的减少。中国近期医药政策环境的调整给医院及医生执业带来一定影响使公司的收入增长放缓。与2022年同期相比,2023年第三季度的产品收入包括:
- 则乐产品收入从3,920万美元增加到4,160万美元,则乐在被纳入国家医保药品目录(NRDL)的第三年,继续保持中国内地卵巢癌领域院内销售领先PARP抑制剂的地位;
- 爱普盾产品收入从1,070万美元增加到1,160万美元,得益于自费患者对该产品可及性的提高;
- 擎乐产品收入从550万美元增加到570万美元,得益于2023年3月被纳入NRDL;
- 纽再乐产品收入从150万美元增加到550万美元,得益于2023年3月被纳入NRDL;
- 卫伟迦产品收入从无增加到490万美元,因其刚于2023年9月上市。
- 则乐产品收入从3,920万美元增加到4,160万美元,则乐在被纳入国家医保药品目录(NRDL)的第三年,继续保持中国内地卵巢癌领域院内销售领先PARP抑制剂的地位;
- 2023年第三季度的研发(R&D)开支为5,880万美元,2022年同期为9,950万美元。研发支出的降低主要原因为与许可及合作协议有关的预付款和里程碑付款减少导致的许可费减少。
- 2023年第三季度的销售、一般和行政开支为6,860万美元,2022年同期为6,660万美元。这一增长主要归因于为支持新产品上市而导致的一般销售费用的增加,部分被专业服务费用减少所抵销。
- 2023年第三季度亏损净额为6,920万美元,每股普通股亏损为0.07美元,2022年同期亏损净额为1.612亿美元,每股普通股亏损为0.17美元。亏损净额减少主要是由于产品收入的增加、许可费的减少以及从汇兑损失转为收益的转换。
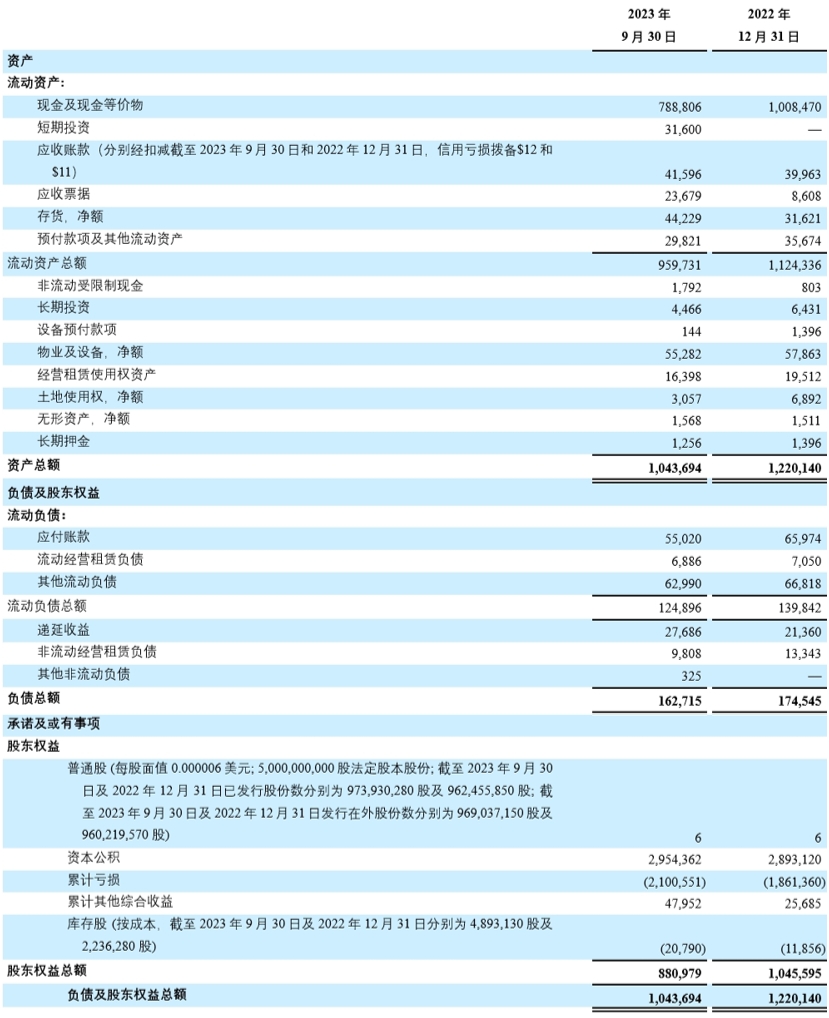
- 截至2023年9月30日,现金及现金等价物、短期投资和受限制现金总计为8.222亿美元,截至2023月6月30日其为8.764亿美元。
近期产品亮点和公司进展
自上次财报发布以来再鼎医药主要产品和公司进展包括:
商业化产品
- 卫伟迦(艾加莫德,FcRn):2023年9月,卫伟迦于中国内地上市,与常规治疗药物联合,用于治疗乙酰胆碱(AChR)抗体阳性的成人gMG患者。再鼎医药的商业化产品数量增加到5款。再鼎医药正努力将卫伟迦纳入NRDL,让这一疗法可以惠及更多患者。
- 则乐(尼拉帕利,PARP):2023年9月,再鼎医药对在中国铂敏感复发性卵巢癌患者中开展的3期NORA研究进行了最终总生存期(OS)分析,分析结果进一步支持了NMPA对则乐在中国用于铂敏感复发性卵巢癌患者的批准。最终OS结果显示,无论患者gBRCA突变状态如何,与安慰剂相比,尼拉帕利用于复发维持治疗表现出了能够延长患者总生存期(OS)的有利趋势。我们期待在即将召开的医学会议上公布详细结果。
肿瘤领域管线
- KRAZATI® (adagrasib, KRASG12C):
- 一线非小细胞肺癌(NSCLC):2023年10月,再鼎医药合作伙伴Mirati Therapeutics(Mirati)在2023年欧洲肿瘤内科学会(ESMO)大会上公布了KRYSTAL-7 2期研究的最新结果,该研究评估了adagrasib联合帕博利珠单抗一线治疗携带KRASG12C突变的NSCLC患者。结果表明,adagrasib与免疫检查点抑制剂联合一线治疗NSCLC具有可控的安全性和持久疗效的初步信号。再鼎医药在中国内地、香港、澳门和台湾地区(统称为大中华区)参与了该研究。
- 二线及以上NSCLC:2023年9月,Mirati在2023年世界肺癌大会(WCLC)上公布了KRYSTAL-1研究的1/1b期队列和2期队列A汇总分析的两年随访数据,该研究针对经治的KRASG12C突变NSCLC患者。在汇总分析中,adagrasib显示出持久的疗效和可控的长期安全性。我们正在大中华区参与对经治的KRASG12C突变NSCLC患者进行的KRYSTAL-12 3期验证性研究。
- 一线非小细胞肺癌(NSCLC):2023年10月,再鼎医药合作伙伴Mirati Therapeutics(Mirati)在2023年欧洲肿瘤内科学会(ESMO)大会上公布了KRYSTAL-7 2期研究的最新结果,该研究评估了adagrasib联合帕博利珠单抗一线治疗携带KRASG12C突变的NSCLC患者。结果表明,adagrasib与免疫检查点抑制剂联合一线治疗NSCLC具有可控的安全性和持久疗效的初步信号。再鼎医药在中国内地、香港、澳门和台湾地区(统称为大中华区)参与了该研究。
- 瑞普替尼(ROS1/TRK):
- NTRK阳性实体瘤:2023年8月,NMPA药品审评中心(CDE)授予瑞普替尼突破性治疗认定(BTD),用于治疗NTRK基因融合的晚期实体瘤患者,这些患者在接受TRK酪氨酸激酶抑制剂(TKIs)治疗后病情出现进展。该BTD是基于1/2期TRIDENT-1研究中全球和中国入组患者的数据支持。
- ROS1阳性NSCLC:2023年8月,再鼎医药合作伙伴百时美施贵宝(BMS)公布了注册性研究TRIDENT-1的最新结果,针对TKI初治或既往接受过一种TKI且未接受过化疗的ROS1阳性局部晚期或转移性NSCLC患者,瑞普替尼继续证实具有高应答率和持久应答,包括良好的颅内应答。再鼎医药正在大中华区参与这项研究。
- 根据TRIDENT-1研究的结果,美国食品药品监督管理局(FDA)受理了BMS提交的瑞普替尼用于ROS1阳性NSCLC的新药上市申请(NDA),并授予其优先审评资格。处方药用户付费方案(PDUFA)目标行动日期为2023年11月27日。
- 再鼎医药向NMPA提交的瑞普替尼用于ROS1阳性NSCLC的NDA已被受理并授予优先审评资格。
- 根据TRIDENT-1研究的结果,美国食品药品监督管理局(FDA)受理了BMS提交的瑞普替尼用于ROS1阳性NSCLC的新药上市申请(NDA),并授予其优先审评资格。处方药用户付费方案(PDUFA)目标行动日期为2023年11月27日。
- NTRK阳性实体瘤:2023年8月,NMPA药品审评中心(CDE)授予瑞普替尼突破性治疗认定(BTD),用于治疗NTRK基因融合的晚期实体瘤患者,这些患者在接受TRK酪氨酸激酶抑制剂(TKIs)治疗后病情出现进展。该BTD是基于1/2期TRIDENT-1研究中全球和中国入组患者的数据支持。
- TIVDAK®(tisotumab vedotin):2023年10月,再鼎医药合作伙伴Seagen Inc.和Genmab A/S 在2023年ESMO 大会上公布了全球3期随机临床研究innovaTV 301的结果,研究显示,与单独化疗相比,在系统治疗期间或治疗后发生疾病进展的复发性或转移性宫颈癌患者中,接受TIVDAK治疗的患者显著地改善了OS、无进展生存期(PFS)和客观缓解率,且未观察到新的安全性信号。我们参与了该全球研究,并正在大中华区开展扩展研究。
- Odronextamab(CD20xCD3):2023年9月,再鼎医药合作伙伴再生元宣布,FDA已受理odronextamab的生物制品许可申请(BLA)并将其纳入优先审评,用于治疗此前至少两次全身治疗后发生进展的复发/难治性(R/R)滤泡性淋巴瘤(FL)或R/R弥漫性大B细胞淋巴瘤(DLBCL)的成年患者,PDUFA目标行动日期为2024年3月31日。2023年8月,欧洲药品管理局(EMA)受理了odronextamab相同适应证的上市申请。
- ZL-1211(Claudin18.2):基于对竞争格局和市场前景的评估,我们决定终止ZL-1211的内部开发。
- 肿瘤电场治疗:2023年8月,再鼎医药合作伙伴NovoCure Limited宣布,肿瘤电场治疗与紫杉醇联合治疗铂耐药卵巢癌患者的3期临床研究INNOVATE-3的最终分析未达到总生存期这一主要终点。再鼎医药未参与这一研究
自身免疫疾病、感染性疾病和中枢神经系统疾病领域管线
- 艾加莫德(FcRn):2023年9月,NMPA药品审评中心授予艾加莫德α注射液(皮下注射)BTD,用于治疗慢性炎性脱髓鞘性多发性神经根神经病(CIDP)患者。该BTD是基于ADHERE研究中全球和中国入组患者阳性数据的支持。
- KarXT (xanomeline-trospium,M1/M4型毒蕈碱乙酰胆碱受体激动剂)
- 精神分裂症:2023年9月,再鼎医药合作伙伴Karuna Therapeutics, Inc. (Karuna)宣布,基于三项注册性研究的阳性数据,已向FDA提交了用于精神分裂症的新药上市申请。再鼎医药将继续为中国内地的注册性桥接研究招募患者。
- 阿尔茨海默症精神病性障碍(ADP):Karuna在第三季度启动了用于ADP的3期临床研究ADEPT-2和ADEPT-3。再鼎医药计划明年在大中华区参与这些研究。
- 精神分裂症:2023年9月,再鼎医药合作伙伴Karuna Therapeutics, Inc. (Karuna)宣布,基于三项注册性研究的阳性数据,已向FDA提交了用于精神分裂症的新药上市申请。再鼎医药将继续为中国内地的注册性桥接研究招募患者。
公司进展
- 组织更新:2023年9月,再鼎医药任命Robert J. Brown博士为肿瘤领域首席医学官。Brown博士是肿瘤药物开发的领导者,拥有超过 16 年的转化、研究和临床开发专业经验。Brown博士将向再鼎医药总裁兼全球肿瘤研发负责人Rafael Amado博士汇报,并为我们肿瘤管线的临床开发提供战略领导和支持。
2023/2024年的预期重要里程碑事件
肿瘤领域
则乐(尼拉帕利,PARP)
- 再鼎医药将在2024年举行的医学会议上公布在中国铂敏感复发性卵巢癌患者中开展的3期NORA研究最终OS分析结果。
肿瘤电场治疗
- NovoCure将于2023年年底前向FDA提交肿瘤电场治疗用于铂类化疗后出现进展的二线及以上NSCLC患者的上市前批准申请。
- NovoCure将于2024年第一季度公布肿瘤电场治疗用于脑转移患者的3期临床研究METIS的主要数据。再鼎医药正在大中华区参与这项研究。
- NovoCure将在2024年下半年公布肿瘤电场治疗用于局部晚期胰腺癌的3期临床研究PANOVA-3的主要数据。再鼎医药正在大中华区参与这项研究。
瑞普替尼(ROS1/TRK)
- 瑞普替尼用于局部晚期或转移性ROS1阳性NSCLC的新药上市申请,有望于2024年获得NMPA批准。
KRAZATI (adagrasib, KRASG12C)
- 再鼎医药将于2024年向NMPA提交adagrasib用于二线及以上KRASG12C突变NSCLC的新药上市申请。
Bemarituzumab (FGFR2b)
- 再鼎医药将于2024年上半年在大中华区加入bemarituzumab联合纳武利尤单抗和化疗用于一线治疗胃癌或胃食管交界处癌的全球3期研究FORTITUDE-102。
ZL-1310 (DLL3 ADC)
- 再鼎医药将于2024年第一季度启动一项ZL-1310用于治疗含铂化疗方案治疗后出现进展的二线及以上复发和难治性小细胞肺癌(SCLC)的全球1期研究。
自身免疫疾病、感染性疾病和中枢神经系统疾病领域
艾加莫德 (FcRn)
- 再鼎医药合作伙伴 argenx将于2023 年第四季度公布艾加莫德皮下注射剂型用于治疗免疫性血小板减少症(ITP)的注册性3 期研究ADVANCE-SC的关键性数据。再鼎医药正在大中华区参与这项研究。
- argenx将于2023年年底左右公布艾加莫德皮下注射剂型用于治疗天疱疮的注册性 3 期研究ADDRESS的关键性数据。再鼎医药正在大中华区参与这项研究。
- argenx 将在 2023 年年底之前提交艾加莫德治疗CIDP的补充 BLA。
- argenx将于2023年第四季度启动艾加莫德治疗甲状腺眼病(TED)的注册性研究。再鼎医药计划2024年在大中华区参与这一项目。
- 艾加莫德皮下注射剂型用于gMG的补充BLA有望于2024年获NMPA批准。
KarXT (xanomeline-trospium,M1/M4型毒蕈碱乙酰胆碱受体激动剂)
- 如KarXT用于精神分裂症的上市申请获得FDA批准,Karuna将于2024年下半年上市KarXT。
- 舒巴坦钠-度洛巴坦钠用于由鲍曼不动杆菌-醋酸钙不动杆菌复合体敏感分离株引起感染的NDA,有望于2024年获NMPA批准。
ZL-1102 (IL-17 Humabody®)
- 再鼎医药将于2024年启动针对慢性斑块状银屑病的全球2期研究。
电话会议和网络直播相关信息
再鼎医药将于美国东部时间2023年11月8日上午8点举行电话会议和网络直播。与会者可以访问公司网站http://ir.zailaboratory.com参与实时网络直播。如要参加电话会议,需提前注册。
详细信息如下:
注册链接:https://register.vevent.com/register/BI87a7a83f6a6441279fddbaae217dd092
所有与会者都必须在电话会议之前通过上方链接完成在线注册。注册成功后,您将收到确认邮件,内含拨入电话会议的具体信息。
会议结束后不久,您可访问再鼎医药官网观看回放。
关于再鼎医药
再鼎医药(纳斯达克股票代码:ZLAB; 香港联交所股份代号:9688)是一家以研发为基础、处于商业化阶段的创新型生物制药公司,总部位于中国和美国。我们致力于通过创新产品的发现、开发和商业化解决肿瘤、自身免疫疾病、感染性疾病和中枢神经系统疾病领域未被满足的巨大医疗需求。我们的目标是利用我们的能力和资源努力促进中国及全世界人类的健康福祉。
有关再鼎医药的更多信息,请访问www.zailaboratory.com或关注公司官微:再鼎医药。
非美国公认会计准则指标
除了根据美国公认会计准则呈现的业绩外,我们还披露了经调整的增长率,以排除由于外币折算为美元产生差异的影响,这是非美国公认会计准则的指标。 我们认为这些非美国公认会计准则指标对于了解我们的经营业绩和财务业绩非常重要,并为投资者提供了趋势的更多视角。尽管我们相信非美国公认会计准则财务指标可以增强投资者对我们业务和业绩的了解,但这些非美国公认会计准则财务指标不应被视为随附美国公认会计准则财务指标的唯一替代指标。
再鼎医药前瞻性陈述
本新闻稿包含了与以下方面相关的前瞻性陈述,包括:我们的策略和计划;我们的业务和管线项目的潜力和预期;临床开发计划和相关临床研究;临床研究数据、数据解读和发布;与药物开发和商业化相关的风险和不确定性;注册相关的讨论、提交、申请、获批和时间线;我们及我们合作伙伴的产品和候选产品的潜在裨益、安全性和疗效;投资、合作和商务拓展活动的预期收益和潜力;我们未来的财务和经营业绩;以及财务指导(包括我们计划的现金来源和用途,以及我们预期实现盈利的途径)。除对过往事实的陈述外,本新闻稿中包含的所有陈述均属前瞻性陈述,并可通过诸如「旨在」、「预计」、「相信」、「有可能」、「估计」、「预期」、「预测」、「目标」、「打算」、「可能」、「计划」、「可能的」、「潜在」、「将会」、「将要」等词汇和其他类似表述予以识别。该等陈述构成《1995年美国私人证券诉讼改革法案》中定义的「前瞻性陈述」。前瞻性陈述并非对未来表现的担保或保证。前瞻性陈述基于我们截至本新闻稿发布之日的预期和假设,并且受到固有不确定性、风险以及可能与前瞻性陈述所预期的情况存在重大差异的情势变更的影响。对于我们在前瞻性陈述中披露的计划、意图、预期或预测,我们可能无法实际实现、执行或满足,请勿过分依赖此等前瞻性陈述。实际结果可能受各种重要因素的影响而与前瞻性陈述所示存在重大差异,该等因素包括但不限于:(1)我们成功商业化自身已获批上市产品并从中产生收入的能力;(2)我们为自身的运营和业务活动获取资金的能力;(3)我们候选产品的临床开发和临床前开发的结果;(4)相关监管机构对我们的候选产品作出审批决定的内容和时间; (5)与在中国营商有关的风险; 和(6)我们向美国证券交易委员会(「SEC」)提交的最新年报和季报以及其他报告中指出的其他因素。我们预计后续事件和发展将导致我们的预期和假设改变,但除法律要求之外,不论是出于新信息、未来事件或其他原因,我们均无义务更新或修订任何前瞻性陈述。该等前瞻性陈述不应被视为我们在本新闻稿发布之日后任何日期的意见而加以信赖。
如需查阅公司向SEC提交的文件,请访问公司网站www.zailaboratory.com和SEC网站www.SEC.gov。
有关更多信息,敬请垂询:
投资者关系:
Christine Chiou / Lina Zhang
+1 (917) 886-6929
christine.chiou1@zailaboratory.com / lina.zhang@zailaboratory.com
媒体:
Shaun Maccoun / Xiaoyu Chen
+1 (415) 317-7255
shaun.maccoun@zailaboratory.com / xiaoyu.chen@zailaboratory.com
再鼎医药有限公司
再鼎医药有限公司
未经审计简明合并资产负债表
(以千美元 ("$")计,股份数目及每股数据除外)
再鼎医药有限公司
未经审计简明合并经营表
(以千$计,股份数目及每股数据除外)
再鼎医药有限公司
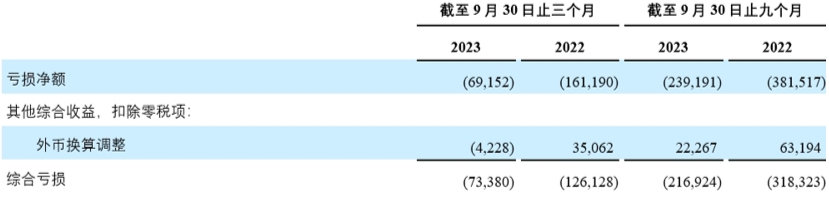
未经审计简明合并综合亏损表
(以千$计)
再鼎医药有限公司
非美国公认会计准则指标
(以千$计)
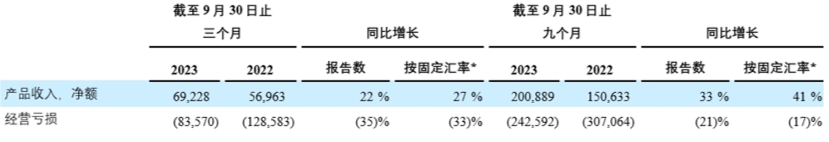
* 按固定汇率计算的增长率是基于当前和上年同期采用相同外币汇率的假设计算得出